Noe å lære av

Anbefaler CPAP ved prehospital håndtering av koronapasienter med lungesvikt
«Vi har nå sett innleggelser av flere pasienter i Oslo-regionen som har et meget aggressivt sykdomsforløp, med rask dekompensasjon og livstruende lungesvikt.»
Vi har de siste dagene gjort oss noen verdifulle erfaringer som vi mener er nyttige å dele med alle i ambulansetjenesten i Norge.
Derfor utgår dette notatet fra Luftambulanseavdelingen ved Oslo universitetssykehus (OUS).
På NAKOS-portalen ligger det nå CPAP kurs med video her
Les også retningslinjene hos NHS (engelsk ambulansetjeneste):Guidance for the role and use of non-invasive respiratory support in adult patients with coronavirus (confirmed or suspected) (v3 6. april)
Bakgrunn
Covid-19 pasientene er en heterogen populasjon, ogsykehistorier og sykdomsutviklingen er mangfoldig. Likevel er det enkelteviktig observasjoner som nå gjøres regelmessig.
Vi har nå sett innleggelser av flere pasienter i Oslo-regionen som har et meget aggressivt sykdomsforløp, med rask dekompensasjon og livstruende lungesvikt. Dette gjelder også relativt unge pasienter 30–60 år, som er friske fra før eller har beskjedne tilleggssykdommer.
Vi vil illustrere dette med en kaustikk og deretternoen læringspunkter og råd om behandling.
Kasuistikk
Luftambulanselege møter ambulanse for å bistå i behandlingen av en kritisk syk covid-19 pasient. Kvinne 67 år, tidligere stort sett frisk, men hypertensjon. Feber og økende pustebesvær siste døgn.
Ambulansen ber om bistand fordi pasienten er i rask forverring og nå knapt orker å trekke pusten. Pasienten har RF 45, Sp0250% med 6 liter på brillekateter. Vi starter støttebehandling med CPAP (Flowsafe II med hepafilter). Gradvis økende flow fra 12 til 25 liter O2.
Behandlingen tolereres meget godt av pasienten som viser tydelig tegn på nedsatt stress og bedring av respirasjon. SpO2 stiger i løpet av 2-3 minutter til over SpO2 >93%.
Patofysiologi
Det patofysiologiske bildet er felles for mange. De har en primær lungesvikt, og er oftest hemodynamisk stabile. Pasientene utvikler det vi kaller en «stille hypoksemi», med gradvis fall i oksygenmetning.
En kompensatorisk rask respirasjonsfrekvens holder CO2-tensjonen lav slik at de ikke får en følelse av åndenød, i motsetning til hva man ofte ser hos pasienter med lungeødem, hjertesvikt, sepsis og pneumoni.
Hypoksi med kompensatorisk lav PaCO2 gir ikke subjektivt ubehag, tvert i mot kan det føles behagelig, pasienten kan miste selvinnsikt og situasjonsforståelse. Forvirring er et vanlig tegn.
Noen har tale-dyspnø, men ikke alle. Pasienten kan høres relativt ubesværet ut ved samtale, men likevel ha alvorlig respirasjonssvikt. Det kliniske bildet kan selvfølgelig variere betydelig, men er ofte annerledes enn det vi ser ved mange andre tilstander (pneumoni, hjertesvikt, lungeemboli, astma).
Videre har de fleste som er friske fra før god hjertefunksjon og opprettholder adekvat blodtrykk på tross av alvorlig hypoksi. På tross av alvorlig lungesvikt har pasientene gjerne relativt bevart compliance i lungene (betyr at lungene er ettergivelige) slik at respirasjonsarbeidet går relativt lett, og de virker derfor ikke nødvendigvis veldig besværet.
Respirasjonsarbeidet vil likevel variere med graden av lungesvikt, og enkelte pasienter er meget slitne på grunn av økt respirasjonsarbeid (høy RF) over flere dager. Ved auskultasjon kan det være fravær av patologiske lungelyder.
Den patofysiologiske mekanismen bak oksygeneringssvikten hos covid-19 pasienter med kritisk lungesvikt er sannsynligvis multifaktoriell. Typisk har disse pasientene god lunge-compliancemed en ren oksygeneringssvikt. En hypoksisk drevet respirasjon med takypne og høyt minuttvolum gir en uttalt hypokapni (lav PaCO2). Det er plausibelt at diffusjonssvikten skyldes interstitielt ødem.
Ødem mellom alveolærmembranen og lungekapillærene øker avstanden oksygenet må diffundere og dermed vil PaO2 falle. I tillegg vil deler av lungene ikke være ventilert, og det foreligger «lunge-shunt». Det betyr at deler av lungene ikke deltar i gassutveksling.
Dette kan skyldes en kombinasjon av atelektaser, og interstitielt ødem. Lungeavsnittene som ikke er ventilert vil fortsatt ha blodgjennomstrømning (perfusjon), men blodet går da utenom («shuntes forbi») friske deler av lungen og vil ikke bli oksygenert, men strømme ut på arteriesiden med uendret lav metning.
Dette betyr at oksygenert blod fra ventilerte deler av lungen blander seg med ikke-oksygenert blod fra fra ikke-ventilerte lungeavsnitt (shunt). Man kan ikke kompensere for slik shunting ved å gi oksygenterapi alene, selv ved administrasjon av 100% oksygen vil pasienten fortsatt ha lav SpO2.
Når man gir et positivt luftveistrykk så rekrutterer man (åpner) lungeavsnitt som ikke er ventilert, dette øker overflaten som er med i gassutveksling og reduserer graden av shunting. Dette er det vi kaller en bedring av forholdet mellom ventilasjon–perfusjon (V/Q).
Oksygenbehandling
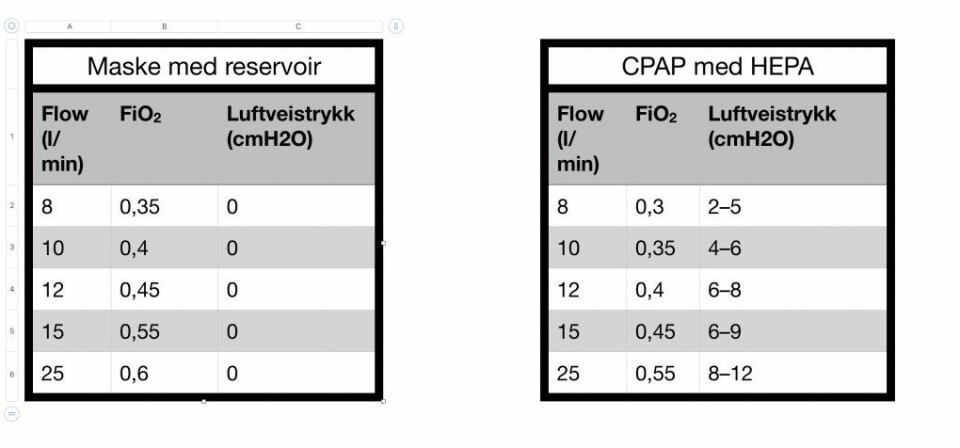
Det er meget viktig med liberal oksygenterapi, og høyflow 12–25 l/min er ofte nødvendig uavhengig av leveringsmetode (brillekateter,maske, CPAP). Disse pasientene responderer fordelaktig på positivtluftveistrykk, og CPAP-behandling er effektivt på tross av at den leverer en FiO2 (fraksjon oksygen) som er noe lavere en maske med reservoar. Vi har utført målinger av FiO2 og luftveistrykk med Flowsafe II CPAP.
Vi har brukt HEPA-filter for å unngå aerosol ut i omgivelsene.
Tabellene under avsnittet viser at CPAP leverer lavere FiO2 sammenliknet med maske med reservoar. Men dette oppveies av at det positive luftveistrykket bedrer lungefunksjonen gjennom rekruttering av områder i lungene som ikke er ventilert.
Vi går derfor ut med en anbefaling om å forsøke CPAP-behandling med 15–25 liter flow om man ikke oppnår SpO2 > 93% med maske eller brillekateter.
Dette vil gi en FiO2 0,45–0,55 og et luftveistrykk på 8–12 cmH20, som i de fleste tilfeller vilvære mer effektivt enn maske med reservoar med FiO2 0,6. CPAP-behandling er fysiologisk plausibelt, og støttes av våre målinger.
Videre er det nå flere leger i Luftambulanseavdelingen som har gode erfaringer med CPAP-behandling av disse pasientene, og liknende erfaringer er rapportert fra andre land. Vi kan ikke se at aerosoldannelse er et problem med tett maske og HEPA–filter. Oksygenmaske med reservoar gir dårligere tetting og luftbåren smitte vil sannsynligvis være et større problem med denne metoden. Vi anbefaler bruk av briller og P3-maske ved all luftveishåndtering.
Behandling

- Pasienten bør sitte oppreist, eller ligge i bratt thoraxleie. Man bør være liberal med oksygenterapi, det vil si inntil 12-15 liter/minutt på maske med reservoar for å oppnå SpO2 > 93%. Hos pasienter som ikke responderer adekvat på dette eller som er utmattet bør man raskt skifte til CPAP-behandling.
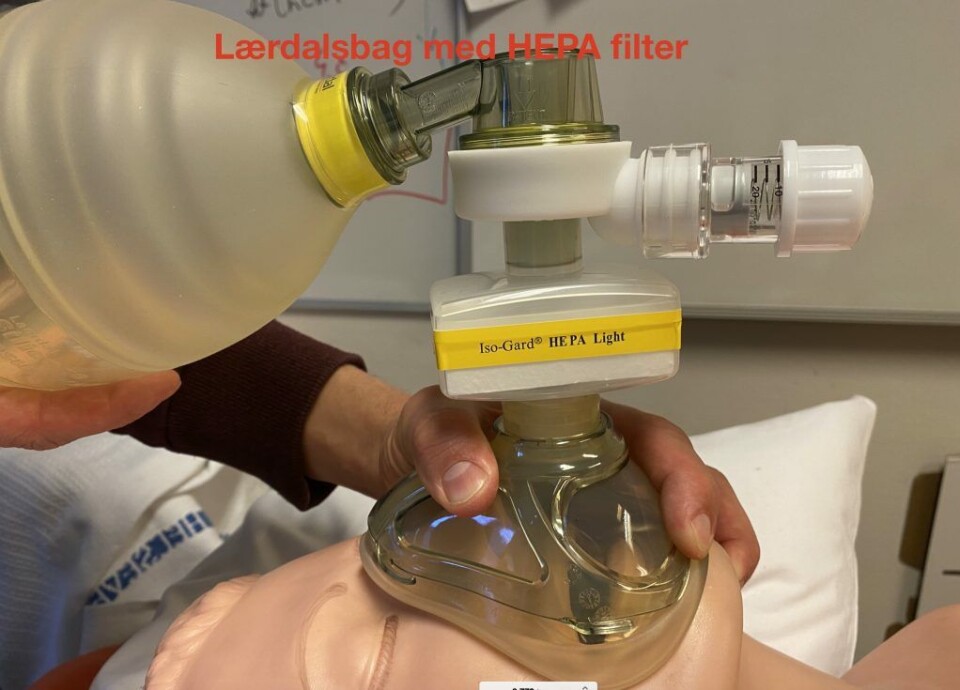
- Start CPAP med 15 l/min og titrer etter respons opp til 25 l/min. Sørg for tett maske. HEPA-filteret skal monteres som vist på bilde. Sørg for at koblingen sitter tett og godt. La pasienten sitte i bratt thoraxleie. Berolige pasienten og hjelp vedkommende å forstå nytten av tiltaket. Ved manglende respons på CPAP-behandling må man varsle LA-lege.
- Om man ikke lykkes med CPAP eller ikke har dette tilgjengelig kan man vurdere å skifte til ventilasjonsbag. Obs! For å minimere aerosoldannelse husk å skru av oksygenet til CPAP masken før du tar den av. Sett deg bak pasienten og holde en ventilasjonsbag med høy flow (12-25 liter/minutt med oksygen) tett rundt pasientens nese og munn. Så lenge reservoirbagen fyller seg så har man tilstrekkelig flow. Ved utilstrekkelig egenrespirasjon bør man støtteventilere pasienten forsiktig. PEEP ventil på ventilasjonsbag er en fordel. Forsøk PEEP 5-10 etter respons. Vær påpasselig med at alle koblinger sitter godt.
- Ved bruk av CPAP eller ventilasjonsbag med høy flow er det viktig at man er bevisst på oksygennivået og følger med på manometer, slik at man kan bytte flaske før den går tom.
- Pasienter med påvirket fysiologi skal behandles varsomt. Disse pasientene kan vise betydelig bedring av fysiologiske parametere i forbindelse med oksygenterapi, men er fortsatt kritisk syke. De bør forflyttes varsomt og må ikke gå selv, eller anstrenge seg på annen måte.
Viktig presisering angående SpO2-måling hos covid-19 pasienter
De sykeste pasienten har en kompensatorisk ventilasjonsrespons med høyt minuttvolum, og hypokapni. Det er rapport om arteriell CO2-tensjon (PaCO2) i området 1,3-2.0 kPa.
En slik ekstrem hypokapni medfører en venstreforskyvning av dissosiasjonskurven for hemoglobin. Ved en venstreforskyvning så øker affiniteten mellom oksygen og hemoglobin (oksygen binder seg lettere til blodet).
Dette medfører at oksygenmetningen for et gitt oksygentrykk blir høyere i en situasjon med hypokapni enn ved hyperkapni.
Med andre ord øker forskjellen mellom arteriell og alveolær oksygentensjon. Dette betyr at en covid-19 pasient med bare moderat nedsatt metning målt ved pulsoksymetri kan ha en forholdsmessig lav arteriell oksygentensjon (PaO2).
Implikasjonene av dette er mange, blant annet vil en tidligere lungefrisk pasient med bare litt redusert SpO2 kanskje være sykere enn vi antar. Måling av ETCO2 vil derfor være veldig nyttig. Ved lav ETCO2 og redusert oksygenmetning kan vi forvente en lavere arteriell oksygentensjon (PaO2) enn SpO2-målingen intuitivt skulle tilsi.
ETCO2 reflekteres bare delvis gjennom respirasjonsfrekvens. Måler man en SpO2 på 95% og en ETCO2 på 2.0 kPa så vil det tyde på at pasienten er sykere enn hva SpO2-verdien skulle tilsi.
Helsedirektoratet har gått ut med en SpO2 < 95% som cut-off verdi hos tidligere lungefriske. Dette virker fornuftig. Lav ETCO2 er i seg selv et bekymringsfullt tegn, og tyder på en kompensatorisk respons på progredierende diffusjonssvikt.
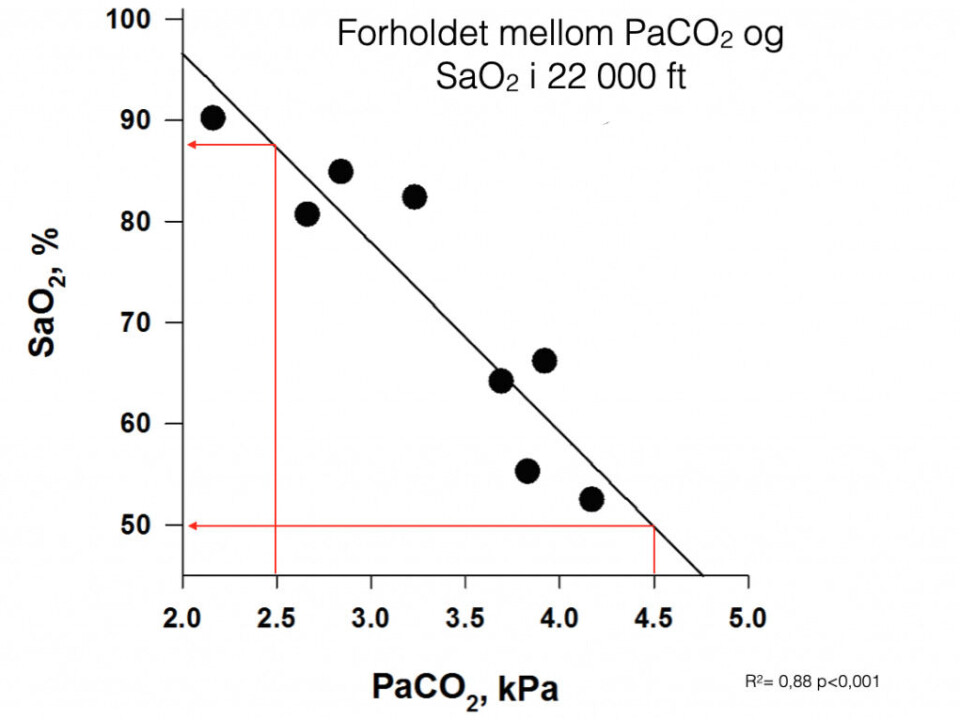
Fysiologien vi har beskrevet kan illustreres med hva som skjer under hypobar hypoksi. I et lavtrykkskammer-forsøk i 22 000 ft høyde målte man både PaCO2 og SaO2. En person med PaCO2 = 4,5 hadde SaO2 = 50%, men en person med PaCO2 = 2,5 hadde en SaO2 = 85%, effekten av hypokapni er derfor betydelig. Les vedlagt artikkel som beskriver denne fysiologien.
Andre momenter
- Vi har eksempler på pasienter som går fra å være fysiologisk upåfallende til å dekompenserer bare få timer senere. Tilbakemelding fra pårørende om at situasjonen forverres bør tas på største alvor. SaO2, RF, HR og blodtrykk må alltid måles uavhengig av klinikk.
- RF > 20 eller Sp02 < 93% hosen ellers lungefrisk person er alvorlig.
- Man må gjøre en observasjon av pasientens respirasjonsarbeid (frekvens, dybde, inndragninger og bruk av hjelpemuskulatur). Ser pasienten sliten ut? Er pasienten medtatt, sliten, eller dehydrert kan situasjonen forverres raskt. Pasientene utvikler gjerne en lungesvikt 5–14 dager etter symptomdebut, med «stille hypoksemi» og rask RF.
- Ved tilbakemelding til luftambulanselege eller sykehusoppgi alltid fysiologiske parametere; RF, SpO2, HR, BT. Pasienter medvedvarende lav metning, eller høy respirasjonsfrekvens på tross avoksygenbehandling bør møtes av team i mottak. Tidlig varsling til sykehus erviktig.
Differensialdiagnostikk
I en tid hvor vår oppmerksomhet er rettet mot covid-19, så må vi ikke glemme viktige differensialdiagnoser slik som lungeemboli, hjerteinfarkt, hjertesvikt, og bakteriell sepsis, som alle gjerne kan komme i forløpet av en langvarig viral infeksjon og komplisere det kliniske bildet.
EKG er en nyttig tilleggsundersøkelse ved differensialdiagnostikk.
Hos pasienter med diabetes må vi ikke glemme blodsukkermåling. Ketoacidose er en livstruende komplikasjon som er assosiert med infeksjoner, og som kan ha et lignende bilde med høy respirasjonsfrekvens.


























